Komplementinhibitoren und Gentherapie: Neue Strategien gegen trockene AMD
Während der Verlauf der feuchten altersabhängigen Makuladegeneration (AMD) heute medikamentös gut abgemildert werden kann, entzieht sich die trockene Form der Erkrankung bislang einer effektiven Therapie. Neue Wirkstoffe aus der Gruppe der Komplementinhibitoren geben nun jedoch Anlass zur Hoffnung, dass auch die trockene Spätform der AMD künftig in ihrem Verlauf gebremst werden kann. Diese Thematik wird auf einem Symposium im Rahmen der DOG diskutiert.
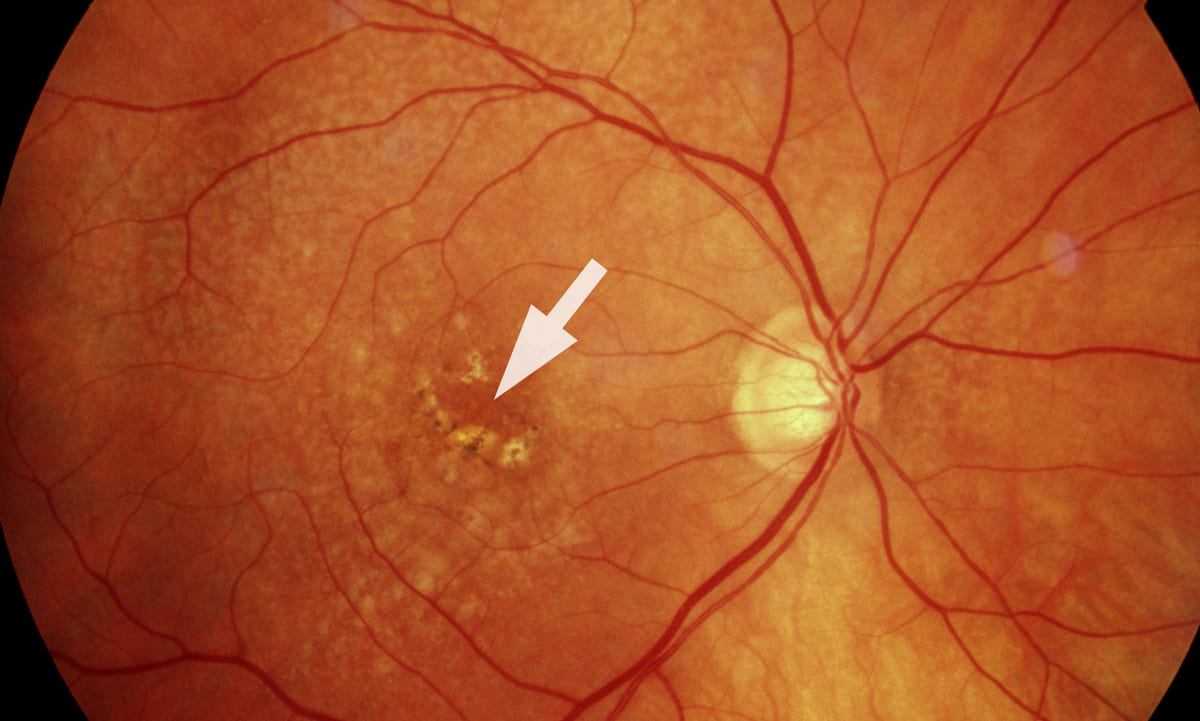
Eine AMD entwickelt sich schleichend: Durchschnittlich zehn Jahre dauert es, bis die Frühform der Erkrankung in die späte AMD übergeht, ab der sich Sehstörungen im Alltag bemerkbar machen. „In dieser späten Phase werden zwei verschiedene Krankheitsformen unterschieden“, erläutert Professor Dr. med. Frank Holz, Direktor der Klinik für Augenheilkunde am Universitätsklinikum Bonn und Vorsitzender der Stiftung Auge. „Die sogenannte feuchte Form, die auf das Aussprossen feinster, undichter Blutgefäße in die Augennetzhaut zurückgeht, und die trockene Form, bei der aufgrund von Ablagerungen unter der Netzhaut die lichtempfindlichen Zellen absterben.“ Seit rund 15 Jahren kann die überschießende Gefäßneubildung bei der feuchten AMD mithilfe von VEGF-Inhibitoren verlangsamt werden. Doch für die trockene Form steht ein vergleichbarer Behandlungserfolg noch aus.
In den vergangenen Jahren sind jedoch die Krankheitsmechanismen, die der trockenen AMD zugrunde liegen, immer besser verstanden worden. „Es sind mittlerweile mehrere Faktoren bekannt, die an dem komplexen Degenerationsprozess in der Netzhaut mitwirken“, sagt Holz. Hierzu zählt die übermäßige Aktivierung des Komplementsystems als Bestandteil der Immunabwehr, die die alternde, sehr stoffwechselaktive Makula mit den chronischen Ablagerungen attackiert. Ein neues Therapiekonzept basiert nun darauf, die Aktivität des Komplementsystems zu hemmen. Zwei der neuen, als Komplementinhibitoren bezeichneten Wirkstoffe haben in Phase 2- bzw. Phase 3-Studien bereits vielversprechende Ergebnisse erzielt. „Die Ausbreitung der Netzhautschäden konnte mit ihrer Hilfe verlangsamt werden“, berichtet Holz. „Einmal untergegangene Sehzellen lassen sich so jedoch nicht regenerieren“, dämpft der DOM-Experte mögliche Erwartungen. Eine Sehverbesserung sei daher nicht zu erzielen.
Die neuen Wirkstoffe wurden im Rahmen der klinischen Studien entweder monatlich oder einmal alle zwei Monate ins Auge gespritzt. Um diese aufwändige Behandlung zu vereinfachen, wird derzeit auch an gentherapeutischen Ansätzen zur Drosselung des Komplementsystems geforscht. „Therapeutische Nukleinsäuren können in einem einmaligen mikrochirurgischen Eingriff in das Auge eingebracht werden“, sagt Holz. Ein entsprechender Wirkstoff befindet sich ebenfalls bereits in der Phase 2 der klinischen Erprobung.
Die Zulassung eines ersten Komplementinhibitors ist im kommenden Jahr möglich. Wenn diese Hürde genommen sei, so Holz, könne in einem nächsten Schritt auch die Anwendung in früheren AMD-Stadien geprüft werden – möglicherweise lasse sich so das Voranschreiten der Erkrankung noch vor den ersten Sehverlusten verhindern.
Dieser Thematik widmet sich das DOG Symposium
Trockene AMD – phänotypische Differenzierung, klinische Endpunkte und Therapieansätze
Termin: Freitag, 30. September 2022, 8.30 bis 9.45 Uhr, hybrid
Die frühen/intermediären nichtexsudativen Manifestationsformen der altersabhängigen Makuladegeneration (AMD) verlaufen progredient hin zu atrophischen und/oder neovaskulären Spätformen. Die geographische Atrophie geht unbehandelt mit einem progredienten irreversiblen korrespondierenden Funktionsverlust einher. Eine präzisere Charakterisierung des natürlichen Verlaufs zusammen mit der Identifikation neuer struktureller und funktioneller Biomarker hat wesentlich zum besseren Verständnis der Erkrankung beigetragen. Hieraus sind u.a. neue Klassifikationssysteme erwachsen (CAM: iRORA/cRORA) sowie strukturelle, funktionelle und patient-reported outcome (PRO) klinische Endpunkte, um Interventionen auch in den früheren Stadien auf ihre Wirksamkeit und Sicherheit hin zu prüfen, womit sich aktuell die europäische MACUSTAR-Studie befasst. Viel Potenzial besitzen hierbei KI-basierte Auswertungs-Algorithmen für die bildgebenden und funktionellen Merkmalsausprägungen. Darüber hinaus lassen sich - z.T. auch basierend auf dem Wissen über die genetischen Faktoren - Risiken modifizieren. Pharmakologische Ansätze mit Komplement-Inhibitoren weisen erstmals auf die Möglichkeit der therapeutischen Verlangsamung der Progression der geographischen Atrophie hin - mit der Aussicht, die foveale Funktion, die häufig initial ausgespart ist („foveal sparing“), länger aufrechtzuerhalten.
Im Rahmen des Symposiums werden diese Aspekte eingehend beleuchtet und diskutiert.
Frank G. Holz (Bonn)
Steffen Schmitz-Valckenberg (Salt Lake City, Vereinigte Staaten)
Robert P. Finger (Bonn)
Quelle: DOG