Gentherapie mit Nebenwirkung: Atrophie nach Behandlung mit Voretigen Neparvovec
Die erste zugelassene Gentherapie mit dem Präparat Voretigen Neparvovec (Luxturna®) markierte den Beginn einer neuen Ära in der Augenheilkunde. Erstmals in Deutschland durchgeführt wurde sie an der Augenklinik der LMU München unter der Leitung von Klinikdirektor Prof. Dr. Siegfried Priglinger im Mai 2019. Doch jetzt informiert das Team in einem Beitrag für Ophthalmology Times Europe, dass Berichte über Netzhautatrophien Bedenken hinsichtlich möglicher Langzeitfolgen der Therapie geweckt haben.

Voretigen Neparvovec (Luxturna®) ermöglicht erstmals die kausale Therapie von Netzhautdystrophien, die auf biallelischen Mutationen im RPE65-Gen beruhen. Die schwerste Verlaufsform dieser Erkrankung ist die Lebersche kongenitale Amaurose (LCA), die bereits bei Geburt oder in den ersten Lebensmonaten auffällt und wie die etwas milderen Verlaufsformen – die early onset retinal dystrophy oder die Verlaufsform der Retinopathia pigmentosa – mit einer ausgeprägten Nachtblindheit einhergeht. Im Verlauf führt die Erkrankung aufgrund der progressiven und irreversiblen Netzhautdegeneration zu einer fortschreitenden Sehminderung bis hin zur kompletten Erblindung.
Ansatzpunkt der Gentherapie sind Mutationen im RPE65 Gen, das für die Bildung des Enzyms Retinoid-Isomerohydrolase kodiert. Voretigen Neparvovec transferiert intakte DNA-Kopien des RPE65 Gens in den Zellkern der Zellen des retinalen Pigmentepithels (RPE). Das Kapsid eines Adeno-assoziierten viralen Vektors vom Serotyp 2 (AAV2) dient dabei als Transportvehikel für die korrekt kodierende Sequenz (cDNA) des humanen RPE65 sowie für weitere regulatorische Elemente. Dieses Prinzip wird Gensupplementation genannt. Behandelte RPE-Zellen können daraufhin wieder funktionstüchtige Retinoid-Isomerohydrolase produzieren. Dieses Protein ist für den physiologischen Sehzyklus unabdingbar. Das Gentherapeutikum wird nach einer Vitrektomie mit einer Injektionskanüle in den subretinalen Raum injiziert. Die Kosten der Einmalbehandlung betragen aktuell ca. 350.000 Euro pro Auge.
Die Gentherapie wurde sowohl von der Europäischen Arzneimittelagentur (2018) als auch von der US-amerikanischen Food and Drug Administration (2017) zugelassen, nachdem die zulassungsrelevante Phase-III-Studie bei den Patienten eine statistisch signifikante Verbesserung des funktionellen Sehvermögens in Form einer erhöhten Lichtempfindlichkeit sowie einer verbesserten Fähigkeit zur Navigation auf einem Bewegungsparcours bei unterschiedlichen Umgebungsbeleuchtungsstärken gezeigt hatte.
Die neue Gentherapie weckt die Hoffnung, eine bislang unheilbare Krankheit mit einem günstigen Nebenwirkungsprofil zu behandeln. Doch wie bei jedem neuen medizinischen Produkt gibt es nur begrenzte Real World Daten, gerade was die Langzeitwirkungen anbetrifft. Jetzt haben Berichte über die Entwicklung postoperativer Netzhautatrophien zu der Besorgnis geführt, dass Voretigen Neparvovec langfristig gravierende Folgen haben könnte.

Anwendung der Gentherapie mit Voretigene Neparvovec. Bild: Augenklinik der LMU München
Bereits die klinischen Zulassungsstudien zeigten, dass mit dem gentherapeutischen Verfahren gewisse Risiken verbunden sind. Die meisten behandlungsbedingten unerwünschten Ereignisse wie beispielsweise ein erhöhter Augeninnendruck, eine Kataraktentwicklung oder ein Reizzustand waren jedoch vorübergehend und/oder nur milde ausgeprägt. Doch jetzt berichtet das Team um Prof. Dr. Siegfried Priglinger, Augenklinik der LMU München, das in Deutschland erstmals Voretigen Neparvovec einsetzte, in Ophthalmology Times Europe über möglicherweise gravierende Folgen dieser Gentherapie: US-amerikanische Kollegen haben eine bislang unbeschriebene Komplikation, die Entwicklung einer chorioretinalen Atrophie, festgestellt. Sie entwickelte sich bei 18 Augen von 10 Patienten – im Durchschnitt 4,7 Monate nach der Behandlung. Trotz der Atrophieentwicklung blieben die funktionellen Ergebnisse bisher bei der Mehrheit der Patienten stabil oder verbesserten sich.
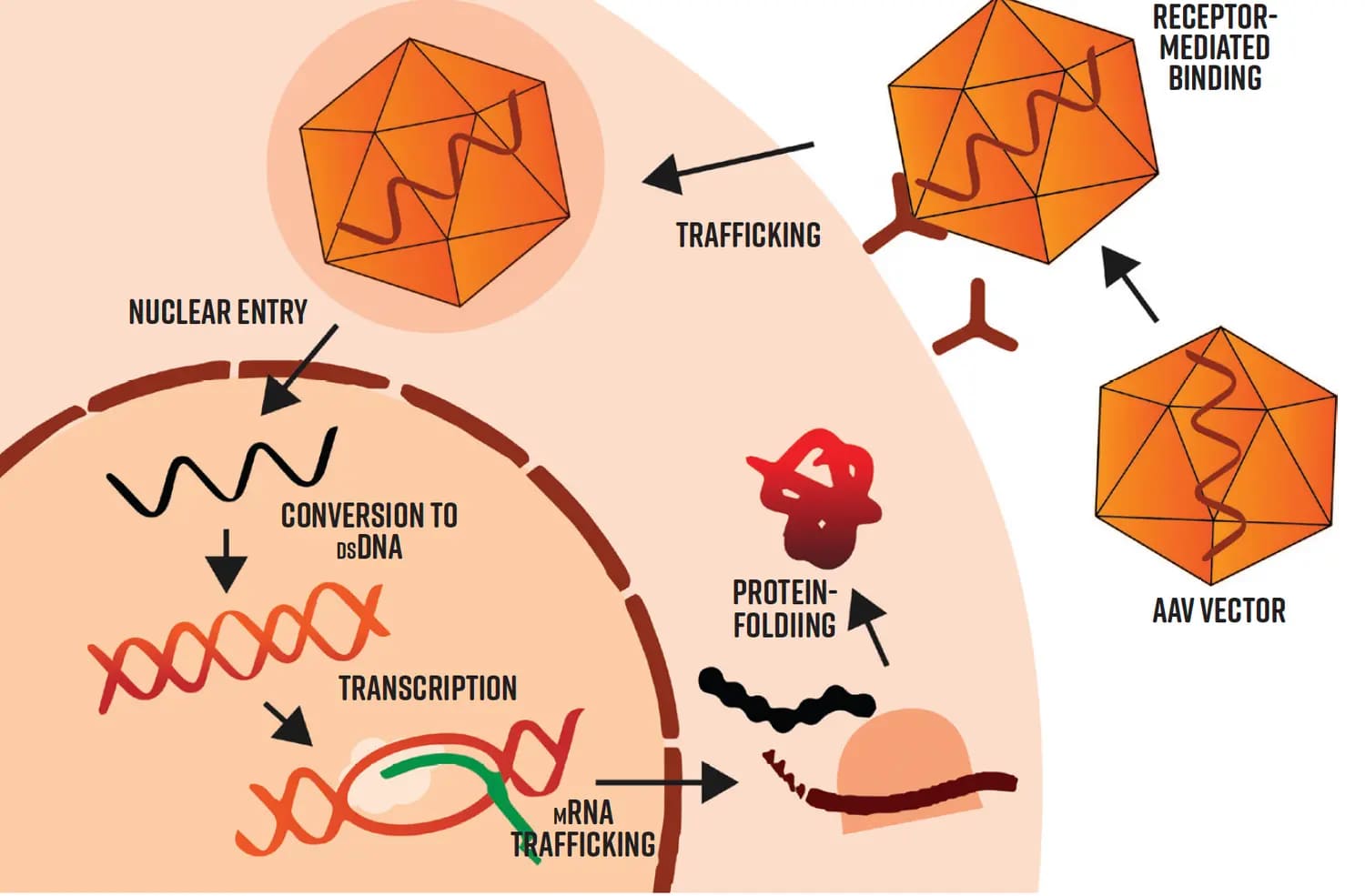
Wirkungsweise der AAV-vermittelten Gentherapie. Bild: Augenklinik der LMU München
In einer weiteren kürzlich erschienenen Publikation wurde über eine fortschreitende Netzhautatrophie bei 13 Augen von 8 Patienten berichtet. Im Monat 3 nach der Therapie wiesen alle 13 Augen Bereiche mit Atrophie auf. Die Ursachen sind noch nicht geklärt. Vermutet werden Immunreaktionen gegen das Vektorgenom oder gegen das Kapsid. Auch chirurgische Faktoren könnten eine wichtige Rolle spielen, ebenso patientenbezogene Faktoren wie Krankheitsstadium, Alter, Geschlecht und Immunstatus.
Die aktuell verfügbaren Daten reichen nicht aus, um eindeutige Schlussfolgerungen über die Ursachen der Atrophieentwicklung und ihre langfristigen funktionellen Folgen zu ziehen. Erfahrungen anderer Behandlungszentren, einschließlich Berichten über das genaue chirurgische Verfahren, sowie längere Nachbeobachtungszeiträume sind notwendig, um ein genaueres Bild über mögliche Auswirkungen der Therapie zu erhalten.
Quellen / mehr Informationen
Ophthalmology Times Europe, August 4, 2022, First-ever retinal gene therapy: Does real-world experience back its use?, Dr Maximilian J. Gerhardt, Prof. Stylianos Michalakis, Prof. Günther Rudolph, Dr Claudia Priglinger, Prof. Siegfried Priglinger
Gange WS, Sisk RA, Besirli CG, et al. Perifoveal Chorioretinal Atrophy after Subretinal Voretigene Neparvovec-rzyl for RPE65-Mediated Leber Congenital Amaurosis. Ophthalmol Retina 2022;6(1):58-64.
Reichel FF, Seitz I, Wozar F, et al. Development of retinal atrophy after subretinal gene therapy with voretigene neparvovec. Br J Ophthalmol 2022.
Zeitschrift Für Praktische Augenheilkunde & Augenärztliche Fortbildung, 10, 2019, Gentherapie bei RPE65-assoziierter Netzhautdystrophie, Siegfried Priglinger, Maximilian Gerhardt, Claudia Priglinger, Günther Rudolph, München
Concept Ophthalmologie, 6/2019, Erste zugelassene Gentherapie für erblich bedingte Netzhauterkrankung in Deutschland durchgeführt, Maximilian Gerhardt