iDose TR: Glaukos gibt positive Ergebnisse in zwei Phase-3-Zulassungsstudien bekannt
Glaukos gab positive Topline-Daten für beide Phase-3-Zulassungsstudien von iDose TR bekannt. In beiden Phase-3-Studien wurden die vordefinierten primären Wirksamkeitsendpunkte nach drei Monaten erfolgreich erreicht und eine ausgezeichnete Verträglichkeit sowie ein günstiges Sicherheitsprofil nach zwölf Monaten nachgewiesen.

iDose TR wird während eines mikroinvasiven Verfahrens verabreicht und enthält eine neuartige Formulierung von Travoprost, einem Prostaglandin-Analogon, das zur Senkung des Augeninnendrucks eingesetzt wird. Sobald Travoprost vollständig freigesetzt ist, kann die iDose TR entfernt und durch eine neue iDose TR ersetzt werden, was eine Alternative zur täglichen Behandlung mit Augentropfen darstellen könnte.
Die wichtigsten Ergebnisse und Beobachtungen aus den Phase-3-Zulassungsstudien mit iDose TR lassen sich so zusammenfassen:
In jeder der beiden Phase-3-Zulassungsstudien mit iDose TR, GC-010 und GC-012, erreichten sowohl der schnell als auch der langsam freisetzende iDose TR-Arm den vordefinierten primären Wirksamkeitsendpunkt der Nicht-Unterlegenheit gegenüber dem aktiven Vergleichsarm (zweimal täglich topische Timolol-Augenlösung, 0,5 %) über 3 Monate.
In der GC-010-Studie betrug die Senkung des Augeninnendrucks gegenüber dem Ausgangswert in den ersten drei Monaten 6,6-8,5 mmHg im iDose TR-Arm mit langsamer Wirkstofffreisetzung gegenüber 6,6-7,7 mmHg im Timolol-Kontrollarm (die mmHg-Spanne stellt die Mittelwerte der Augeninnendrucksenkung über die sechs von der FDA vorgegebenen Zeitpunkte 8 Uhr und 10 Uhr an Tag 10, Woche 6 und Monat 3 dar). In der GC-012-Studie betrug die Senkung des Augeninnendrucks gegenüber dem Ausgangswert in den ersten drei Monaten 6,7-8,4 mmHg im iDose TR-Arm mit langsamer Wirkstofffreisetzung gegenüber 6,8-7,2 mmHg in der Timolol-Kontrollgruppe.
93 % der Probanden, die iDose TR mit langsamer Wirkstofffreisetzung erhielten, waren nach 12 Monaten im Vergleich zum Screening nach einmaliger Verabreichung von iDose TR weiterhin gut auf dieselben oder weniger IOD-senkende topische Medikamente eingestellt, gegenüber 67 % der Timolol-Kontrollprobanden in beiden Phase-3-Studien. Darüber hinaus kamen 81 % der Probanden, die iDose TR mit langsamer Wirkstofffreisetzung erhielten, nach 12 Monaten in beiden Studien ohne IOD-senkende topische Arzneimittel aus.
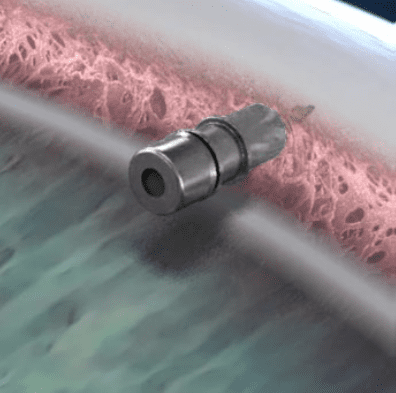
iDose TR. Bilder: Glaukos
iDose TR zeigte eine ausgezeichnete Verträglichkeit: 98 % der Probanden mit iDose TR mit langsamer Wirkstofffreisetzung nahmen nach 12 Monaten weiter an der Studie teil, gegenüber 95 % der Probanden der Timolol-Kontrollgruppe in beiden Phase-3-Studien.
iDose TR wies über 12 Monate ein günstiges Sicherheitsprofil auf, ohne dass es zu einem Verlust von Hornhautendothelzellen, zu schwerwiegenden, die Hornhaut betreffenden Nebenwirkungen und zu einer periorbitalen Fettatrophie kam. Insbesondere trat bei den Probanden, die iDose TR mit langsamer Wirkstofffreisetzung erhielten, eine Hyperämie der Bindehaut mit einer sehr geringen Rate von 3 % auf. Das häufigste unerwünschte Ereignis bei Probanden, die iDose TR mit langsamer Wirkstofffreisetzung erhielten, war eine leichte, vorübergehende Iritis mit einer Rate von 6 % in beiden Phase-3-Studien.
Die Verabreichung von iDose TR in der Praxis wurde bei verschiedenen Probanden an mehreren Standorten erfolgreich durchgeführt, wobei die Ergebnisse mit denen der Phase-3-Studien übereinstimmten, was die Durchführbarkeit der Verabreichung von iDose TR in der Praxis beweist.
"Wir freuen uns sehr, diese robusten und replizierbaren positiven Phase-3-Zulassungsdaten für iDose TR bekannt geben zu können. Sie stellen einen wichtigen Meilenstein für unser Unternehmen dar und bestätigen nachdrücklich unsere Ansicht, dass iDose TR eine transformative, neuartige Technologie sein kann, die in der Lage ist, das Behandlungsparadigma für Glaukompatienten grundlegend zu verbessern", sagte Thomas Burns, Chairman und Chief Executive Officer von Glaukos, in einer Pressemitteilung des Unternehmens. "Wir glauben, dass es in der Augenheilkunde einen großen ungedeckten klinischen Bedarf und ein starkes Interesse an sicheren, wirksamen und nachhaltigen pharmazeutischen Alternativen zu herkömmlichen topischen Medikamenten gibt. Mit diesen Daten sind wir in einer idealen Position für die bevorstehende Einreichung des Zulassungsantrags und die Prüfung durch die FDA für iDose TR."
Basierend auf den kombinierten Wirksamkeits- und Sicherheitsergebnissen der beiden Phase-3-Zulassungsstudien plant Glaukos, seine Pläne für einen NDA-Antrag bei der FDA für das langsam freisetzende iDose TR-Modell voranzutreiben, wobei die Prüfung und Entscheidung der FDA bis Ende 2023 abgeschlossen sein soll.
Quelle: Glaukos