Netzhautschädigung durch Diabetes besser verstehen
Erstmals gelang Wiener Forschern der Nachweis eines bisher nur vermuteten Zusammenhangs: Verminderter Sauerstofftransport in die Netzhaut aufgrund von Schäden an den feinen Blutgefäßen führt zu diabetischer Retinopathie. Bereits bevor sich die Sicht verschlechtert, ist der Gasaustausch im Auge eingeschränkt.
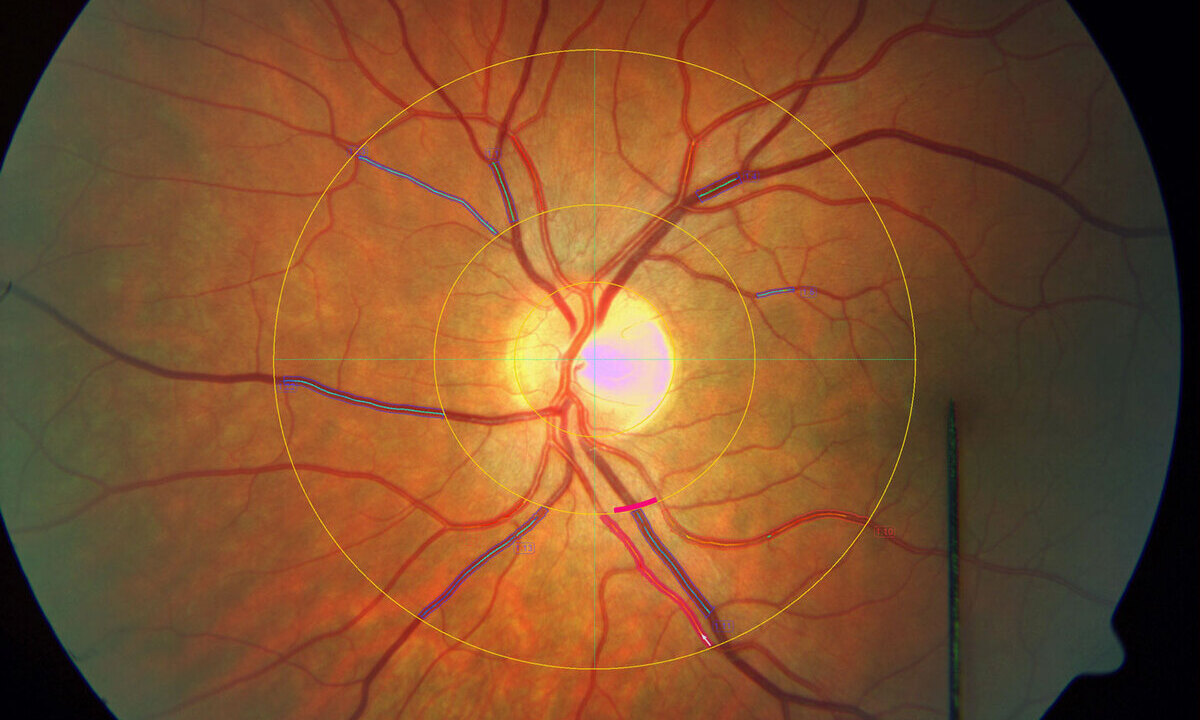
Für den klinischen Pharmakologen Assoc. Prof. Dr. Gerhard Garhöfer von der Medizinischen Universität Wien ist das Auge „ein Fenster zur Mikrozirkulation in den feinsten Blutgefäßen“. Denn nicht nur Augenerkrankungen, sondern auch diverse andere Krankheiten können sich am Zustand der Blutgefäße zeigen. So auch Diabetes Typ 2. Garhöfers Arbeitsgruppe ist es mit Unterstützung des Wissenschaftsfonds FWF gelungen, den bisher nur vermuteten Zusammenhang zwischen vermindertem Sauerstofftransport in der Netzhaut und diabetischer Retinopathie zu belegen. Diabetische Retinopathie tritt bei rund der Hälfte der Patient:innen mit Diabetes Typ 2 auf, die lange erkrankt und/oder schlecht eingestellt sind.
Untersucht wurden für die klinische Studie Typ-2-Diabetiker:innen ohne und mit unterschiedlich stark fortgeschrittener Netzhautschädigung. Die 70 Patient:innen waren im Schnitt 65 Jahre alt und wurden verglichen mit einer 20-köpfigen Kontrollgruppe ohne Diabetes. Da die Sauerstoffaufnahme aus dem Blut ins Gewebe nicht direkt gemessen werden kann, wurden Durchblutung und Sauerstoffsättigung in der Retina der Patient:innen berührungslos gemessen. In einem Vorprojekt wurde bereits ein mathematisches Modell entwickelt, das die Daten der Messungen mittels Doppler Optischer Koheränztomografie und Oximetrie in Werte für die Sauerstoffaufnahme im Gewebe umrechnet.
Die Untersuchungen belegen den bisher nur vermuteten Zusammenhang deutlich: „Unsere Ergebnisse zeigen, dass mit zunehmender Schwere der Erkrankung immer weniger Sauerstoff den Weg vom Blut ins Gewebe findet. Andererseits zeigte sich, dass auch bei Typ-2-Diabetiker:innen, die noch keine sichtbaren Veränderungen der Netzhaut zeigten, bereits weniger Sauerstoff den Weg in die Retina findet. Bevor sie klinisch diagnostizierbar waren, war also der Gasstoffwechsel bereits gestört.“
Pathophysiologie als Basis der Behandlung
Gerhard Garhöfer arbeitet an der Universitätsklinik für Klinische Pharmakologie der Medizinischen Universität Wien, die Wirkstoffe, Behandlungswege und Heilmittel erforscht und entwickelt. Seine Arbeitsgruppe zum Thema „Augen-Pharmakologie“ ist aufgrund der „Fensterfunktion“ des Auges für viele Fachgebiete interessant. „Um Krankheiten gut behandeln zu können, müssen wir ihre Entstehung und ihr Voranschreiten verstehen. Unsere Forschung hat die Pathophysiologie des Auges bei Diabetes weiter entschlüsselt“, erklärt Garhöfer. Die Studienergebnisse bestätigen, dass bei Typ-2-Diabetiker:innen die Sauerstoffabgabe in die Netzhaut reduziert ist. Die gemessenen Parameter könnten dabei helfen, Hochrisikopatient:innen zu identifizieren und im Hinblick auf Therapie und deren Einhaltung besser zu schulen. Gerhard Garhöfer plant, diese Technik auch auf andere Erkrankungen, beispielsweise neurodegenerative Erkrankungen des Auges, anzuwenden.
Zur Person
Assoc. Prof. Dr. Gerhard Garhöfer ist Facharzt für Augenheilkunde an der Medizinischen Universität Wien. Er leitet die Arbeitsgruppe „Ophthalmologische Pharmakologie“ mit den Schwerpunktthemen Arzneimittelentwicklung für das Auge, das Auge als Verabreichungsweg sowie Physiologie und Pharmakologie des Auges. Der assoziierte Professor für Klinische Pharmakologie war Vizepräsident der European Association for Vision and Eye Research (EVER) und ist aktuell Mitglied im Executive Board der European Glaucoma Society (EGS).
Quelle
FWF (Fonds zur Förderung der wissenschaftlichen Forschung)
Publikationen
Hommer N., Kallab M., Schlatter A. et al.: Retinal Oxygen Metabolism in Patients with Type II Diabetes and Different Stages of Diabetic Retinopathy, in: Diabetes 202
Hommer N., Kallab M., Schlatter A. et al.: Neuro-vascular coupling and heart rate variability in patients with type II diabetes at different stages of diabetic retinopathy, in: Frontiers in Medicine (Lausanne) 2022