Mechanismus entschlüsselt: So entstehen Synapsen
Wie entstehen eigentlich Synapsen? Wissenschaftler vom Leibniz-Forschungsinstitut für Molekulare Pharmakologie haben jetzt zusammen mit einem internationalen Team einen entscheidenden Mechanismus aufgedeckt und die Identität der axonalen Transportvesikel aufgeklärt. Die Erkenntnisse liefern wichtige Grundlagen, um künftig die Regeneration von Nervenzellen zu befördern oder auch Alterungsprozessen entgegenzuwirken.
Im Fachmagazin Science wurden die Ergebnisse soeben vorgestellt.
Ob im Gehirn oder in der Muskulatur – überall dort, wo sich Nervenzellen befinden, gibt es auch Synapsen. Die Kontaktstellen der Nervenzellen bilden die Grundlage für die Erregungsübertragung, also die Kommunikation der Nervenzellen untereinander. Wie in jedem Kommunikationsprozess gibt es auch hier einen Sender und einen Empfänger: als Sender fungieren dabei die Axone, welche elektrische Signale generieren und übertragen. Synapsen stellen Kontaktstellen zwischen axonalen Nervenendigungen (die Präsynapse) und postsynaptischen Neuronen dar. An diesen Synapsen wird das elektrische Signal in chemische Botenstoffe umgewandelt, die dann von den Postsynapsen anderer Nervenzellen empfangen werden. Die Freisetzung der Botenstoffe erfolgt aus speziellen Membranbläschen, den sogenannten synaptischen Vesikeln.
Neben der Übertragung von Erregung können Synapsen auch Informationen speichern. Während Aufbau und Funktionen von Synapsen gut verstanden sind, weiß man wenig darüber, wie sie eigentlich entstehen.
Ein Team vom Leibniz-Forschungsinstitut für Molekulare Pharmakologie (FMP) in Berlin hat nun große Teile dieses Rätsels gelüftet. An der bemerkenswerten Arbeit waren außerdem Wissenschaftler der Charité-Universitätsmedizin, dem Max-Delbrück-Centrum für Molekulare Medizin (MDC) und den Universitäten Leipzig, Chicago und Sheffield beteiligt.
Leuchtendes Protein zeigt den Werdegang von synaptischen Vesikeln
Um die Entstehung von Präsynapsen von Anfang an nachverfolgen zu können, haben die Forschenden in humanen Stammzellen per Genschere CRISPR ein leuchtendes Protein eingebaut und aus den so modifizierten Stammzellen Nervenzellen generiert. Dank der Leuchtmarkierung konnten sie nun den Entwicklungsprozess der werdenden synaptischen Vesikel in lebenden Zellen direkt im Mikroskop beobachten.
Synaptische Vesikel sind jene Membranbläschen, welche die Botenstoffe enthalten und die jede Synapse auf Vorrat anlegt, damit sie elektrische Signale in chemische umwandeln kann. Zusammen mit Gerüstproteinen, die den synaptischen Vesikeln sagen, wo sich die Synapse befindet, und Kalziumkanälen, die das elektrische Signal chemisch übersetzen, bilden diese Bläschen die zentralen Bausteine der Präsynapse.
Alle drei Komponenten haben ihre eigenen Gene und bestehen dementsprechend aus unterschiedlichen Eiweißmolekülen. Deswegen dachte man bislang, dass sie auch unterschiedliche Wege nehmen, um schließlich an einem Ort zusammenzukommen und dort eine funktionale Synapse zu bilden.
Alle Komponenten machen sich gemeinsam auf den Weg
Doch diese Annahme konnten die Forschenden durch ihre Beobachtungen widerlegen. „Die synaptischen Vesikelproteine und die Proteine der sogenannten aktiven Zone ebenso wie die Adhäsionsproteine, die die Synapse zusammenkleben, nehmen alle den gleichen Bus“, beschreibt Forschungsgruppenleiter Prof. Dr. Volker Haucke den überraschenden Befund. „Das war sehr umstritten. Unsere Daten in humanen Nervenzellen in Kultur sind aber recht eindeutig.“
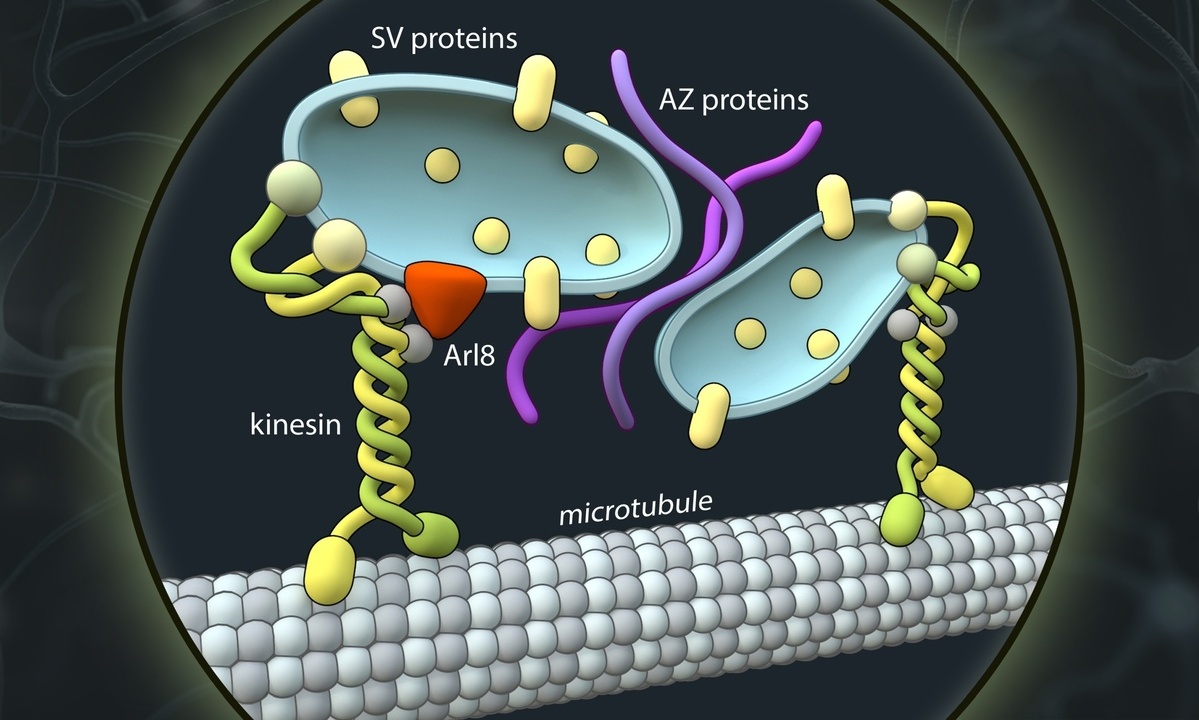
Doch wie genau kommen die Proteine nun an den Ort, an dem die Synapse gebildet wird? In der Arbeit konnten die Forschenden zum einen darlegen, dass für den axonalen Transport eine Maschinerie aus Motorproteinen angeworfen wird. Der Haupttreiber ist demnach das sogenannte Kinesin „KIF1A“. Dieses Motorprotein ist vor allem im Zusammenhang mit neurologischen Störungen im peripheren Nervensystem und im Gehirn bekannt. „Wir vermuten, dass Mutationen in KIF1A den axonalen Transport präsynaptischer Proteine behindern und es so zu neurologischen Symptomen wie Bewegungsstörungen, Ataxie oder geistigen Behinderungen kommt", erläutert Volker Haucke. Der Wissenschaftler ist auch Professor für Molekulare Pharmakologie an der Freien Universität Berlin.
Aber auch die zellbiologische Identität des eigentlichen Transportmittels konnten die Forschenden bestimmen. Und wieder gab es eine Überraschung: Während die allermeisten sekretorischen Vesikel aus dem sogenannten Golgi-Apparat stammen, haben diese axonalen Transportvesikel keine Golgi-Markierung, sondern teilen sich Markierungen mit dem endolysosomalen System, das in anderen Zellen den Abbau von defekten Proteinen bewirkt. Es war eine neuartige Verknüpfung aus Licht- und hochauflösender Elektronenmikroskopie, die es den Forschenden ermöglichte, die axonalen Transportvesikel ultrastrukturell anzuschauen, das heißt auch ihre Größe und Form zu beschreiben.
Transportorganellen entdeckt, die es nur in Nervenzellen gibt
„Unsere Arbeit legt nahe, dass Neuronen eine Art neue Organelle erfunden haben, eine Transportorganelle, die es wahrscheinlich in dieser Form nur in Nervenzellen gibt“, erläutert Dr. Sila Rizalar, FMP-Postdoc und Erstautorin der in „Science“ publizierten Arbeit. „Das wusste man vorher ebenso wenig, wie man den gemeinsamen Transportweg kannte.“
Die neuen Erkenntnisse aus der Grundlagenforschung könnten eines Tages auch für die Klinik nützlich sein. Denn wenn die Kontakte zwischen den Nervenzellen kaputtgehen, sei es durch eine Krankheit, einen Unfall oder schlicht durch den Alterungsprozess, ist es wichtig, den Mechanismus des axonalen Transports und die beteiligten Schlüsselproteine zu kennen, um therapeutisch eingreifen zu können. „Im Idealfall wird man in der Lage sein, diesen axonalen Transport wiederzubeleben oder zu verstärken, um damit Regeneration von Nervenzellen zu befördern oder Alterungsprozessen entgegenzuwirken“, sagt Volker Haucke.
Obwohl die Forschenden nun einen entscheidenden Mechanismus der Synapsenentstehung entschlüsselt haben, sind noch viele Fragen offen. Zum Beispiel, wie die neu entdeckten Transportorganellen eigentlich entstehen, aus was sie gebaut sind oder wie sie ihre Fracht, die Synapsenmoleküle, am Ort ihrer Bestimmung abliefern. Auch steht die Frage im Raum, ob lebenslange Erinnerungen nicht möglicherweise über den gleichen axonalen Transportmechanismus abgespeichert werden, der für die Bildung von Synapsen verantwortlich ist. All diese Fragen will das Team um Volker Haucke nun weiterverfolgen. Es bleibt also spannend.
Quelle: Leibniz-Forschungsinstitut für Molekulare Pharmakologie (FMP)
Originalpublikation:
Filiz Sila Rizalar, Max T. Lucht, Astrid Petzoldt, Shuhan Kong, Jiachen Sun, James H. Vines, Narasimha Swamy Telugu, Sebastian Diecke, Thomas Kaas, Torsten Bullmann, Christopher Schmied, Delia Löwe, Jason S. King, Wonhwa Cho, Stefan Hallermann, Dmytro Puchkov, Stephan J. Sigrist, Volker Haucke. Phosphatidylinositol 3,5-bisphosphate facilitates axonal vesicle transport and presynapse assembly. Science