G-BA: Erneute Zusatznutzenbewertung von Tebentafusp nach Erreichen der Umsatzschwelle
Bei der erneuten Nutzenbewertung von Orphan Drugs im Vergleich zur zweckmäßigen Vergleichstherapie bestätigt der Gemeinsame Bundesausschuss (G-BA) für den Wirkstoff Tebentafusp bei uvealem Melanom einen beträchtlichen Zusatznutzen.
Anlass der Neubewertung war, dass die Umsatzgrenze mit der gesetzlichen Krankenversicherung einen Betrag von 30 Millionen Euro überschritten hatte. Bis zum Erreichen dieser Umsatzgrenze gilt der Zusatznutzen bereits auf Grundlage der Zulassung für seltene Erkrankungen nach dem Willen des Gesetzgebers als belegt. Der G-BA bewertet – sofern der pharmazeutische Unternehmer nicht von sich aus eine reguläre Bewertung des Zusatznutzens gegenüber einer vom G-BA bestimmten zweckmäßigen Vergleichstherapie in Anspruch nimmt – nur das Ausmaß des unter Berücksichtigung der Zulassung anzunehmenden Zusatznutzens.
Tebentafusp: Gute Studie bestätigt beträchtlichen Zusatznutzen
Tebentafusp ist zugelassen zur Behandlung von HLA (humanes Leukozyten-Antigen)-A*02:01-positiven Erwachsenen mit einem inoperablen oder metastasierten uvealen Melanom. Der G-BA konnte für das Orphan Drug auf Basis einer noch laufenden, randomisierten, multizentrischen Studie auch im Vergleich gegenüber einer Therapie nach ärztlicher Maßgabe einen beträchtlichen Zusatznutzen feststellen. Ausschlaggebend für die Bestätigung des festgestellten Zusatznutzens aus dem Jahr 2022 ist ein deutlicher positiver Effekt für die Dauer des Überlebens, der für die Patientinnen und Patienten in einer fortgeschrittenen palliativen Behandlungssituation auch gegenüber der zweckmäßigen Vergleichstherapie gezeigt wird.
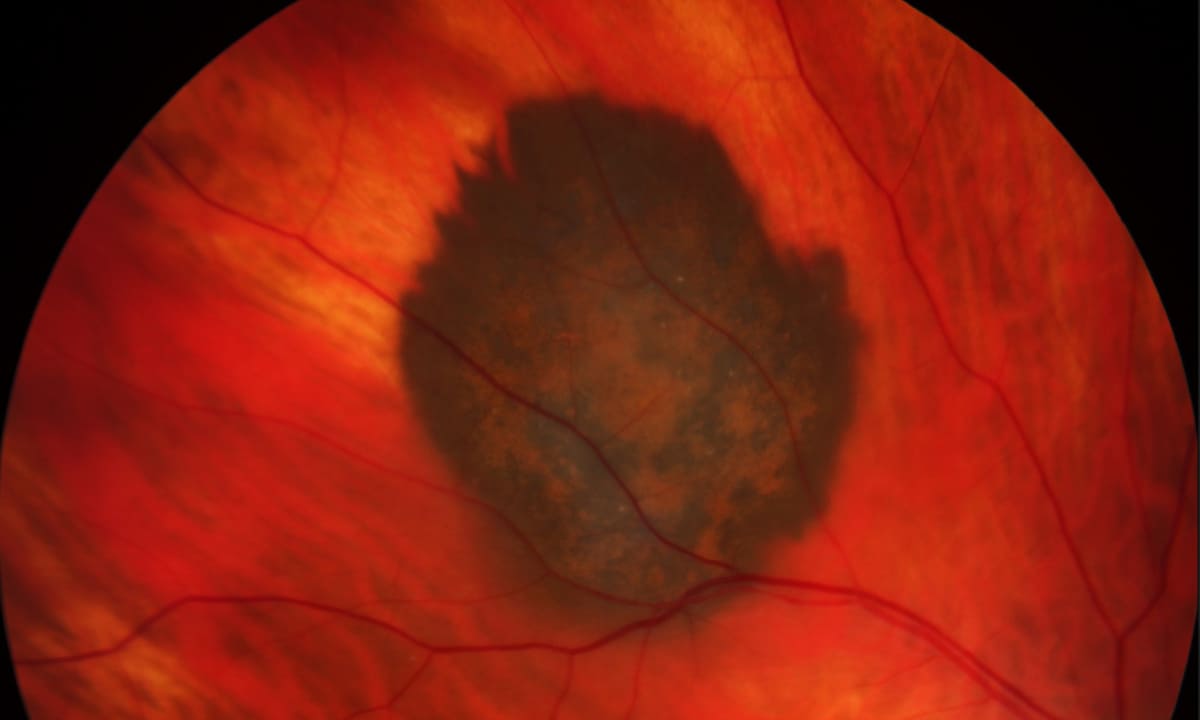
Tebentafusp (Kimmtrak®) von Immunocore ist die erste zugelassene Therapieoption mit neuer Wirkungsweise bei inoperablem oder metastasiertem uvealen Melanom. Das Fusionsprotein stellt eine immunologische Synapse zwischen Krebszelle und Immunsystem her, wodurch die Zerstörung der Tumorzelle aktiviert wird. Die Arznei erhielt jetzt den Galenus-Preis in der Kategorie Orphan Drugs.
2023 wurde Kimmtrak® in der Kategorie Orphan Drugs mit dem Galenus-von-Pergamon-Preis des Springer Medizin Verlags ausgezeichnet.