Wie verletzte Nerven sich selbst am Heilen hindern
Schädigungen von Nervenfasern im Zentralen Nervensystem – Gehirn, Sehnerv oder Rückenmark – ziehen oft lebenslange und schwerwiegende Behinderungen nach sich. Ein Forschungsteam der Ruhr-Universität Bochum (RUB) entdeckte jetzt am Modell des Sehnervs eine überraschende Ursache für das Ausbleiben der Regeneration im ZNS. Daraus könnten sich neue Ansätze für die Entwicklung von Medikamenten ergeben.
Drei wesentliche Ursachen für die Regenerationsunfähigkeit verletzter Nerven des ZNS waren bislang bekannt:
- die unzureichende Aktivierung eines Regenerationsprogramms in verletzten Nervenzellen, welche das Faserwachstum anregt
- die Ausbildung einer für Nervenfasern nur schwer zu durchdringenden Narbe an der Verletzungsstelle
- eine hemmende Wirkung von Eiweißmolekülen im Nerven auf die Axone.
„Wenngleich man in den vergangenen Jahrzehnten experimentelle Ansätze gefunden hat, auf diese einzelnen Aspekte therapeutisch einzugehen, zeigten selbst kombinatorische Ansätze nur einen mäßigen Erfolg“, so Prof. Dr. Dietmar Fischer vom Lehrstuhl für Zellphysiologie der RUB, der Leiter des Forschungsteams. „Es muss also noch weitere, bisher unbekannte Ursachen dafür geben, warum Nervenfasern im ZNS nicht regenerieren.“
Sein Team konnte nun am Modell des Sehnervs eine weitere, für die Forschenden überraschende Ursache für das Ausbleiben der Regeneration im ZNS zeigen. Der zugrunde liegende Mechanismus basiert nicht wie bei den bisher bekannten Gründen auf einer Hemmung des Faserwachstums, sondern vielmehr auf einer positiven Wirkung eines Proteins an der Verletzungsstelle des Nervs. Dieses Molekül ist ein Chemokin mit der Bezeichnung CXCL12. „Das Protein fördert eigentlich das Wachstum von Axonen und lockt regenerierende Fasern an. Es ist also chemoattraktiv“, erklärt Fischer. Genau diese Eigenschaft entpuppte sich aber bei der Regeneration im lebenden Tier als großes Problem.
Gefangene Nervenfasern
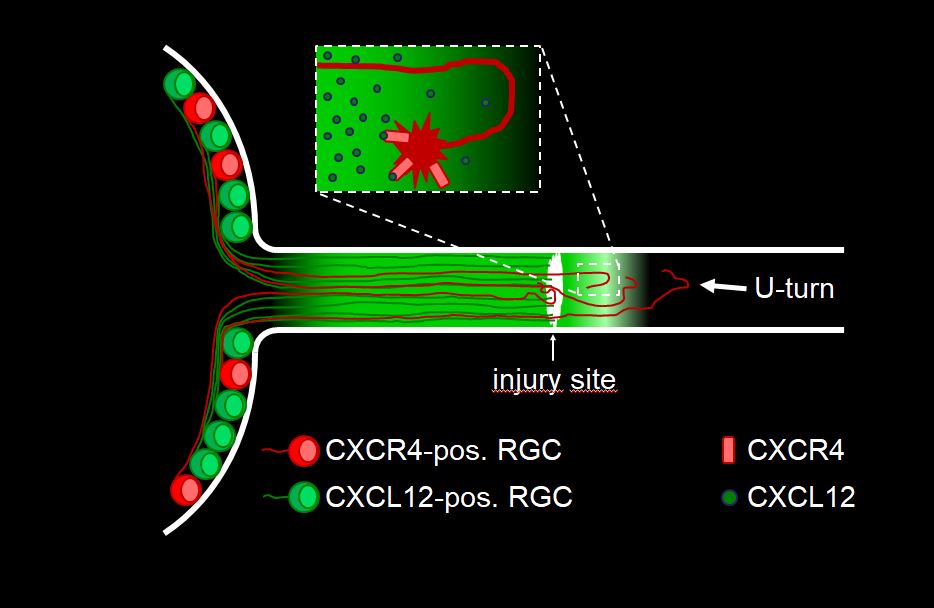
Die Bochumer Forschenden konnten zeigen, dass dieses Protein an der Verletzungsstelle im Nerven freigesetzt wird und somit die Axone durch den chemoattraktiven Effekt an der verletzten Stelle hält. Einige Fasern, die bereits über die Verletzungsstelle hinweg regeneriert waren, wechselten dadurch sogar die Richtung und wuchsen wieder zurück zur Verletzungsstelle. Die nachwachsenden Fasern blieben also durch die Anziehung von CXCL12 an der Verletzungsstelle gefangen.
Sie kamen diesem Effekt auf die Schliche, als sie den Rezeptor für CXCL12, der CXCR4 genannt wird, gezielt in den Nervenzellen der Netzhaut eliminierten und damit blind für dieses Protein machten. „Überraschenderweise führte dies zu einem stark gesteigerten Faserwachstum in den verletzten Sehnerven, und Axone zeigten ein deutlich geringeres Zurückwachsen zur Verletzungsstelle“, berichtet Dietmar Fischer.
Ansatzpunkt für neue Medikamente
Die Forschenden gingen daraufhin der Frage nach, woher das CXCL12 an der Verletzungsstelle stammt. Dabei fanden sie heraus, dass etwa acht Prozent der Nervenzellen in der Netzhaut selbst dieses Protein produzieren, es entlang ihrer Fasern zur Verletzungsstelle im Sehnerven transportieren und es dort aus den durchtrennten Axonen freisetzen. „Es ist noch völlig unbekannt, warum einige dieser Nervenzellen CXCL12 und andere den Rezeptor bilden“, so Fischer. „Wir kennen die physiologische Rolle des Proteins noch nicht, sehen aber, dass es für die Reparatur des Nervensystems sehr hinderlich ist.“
In weiterführenden Experimenten zeigten die Bochumer Wissenschaftler, dass auch die Ausschaltung von CXCL12 selbst in den Nervenzellen der Netzhaut gleichermaßen die axonale Regeneration in den Sehnerv verbesserte. „Diese neuen Erkenntnisse eröffnen uns nun die Möglichkeit, pharmakologische Ansätze zu entwickeln, die darauf abzielen, die Interaktion von CXCL12 und seinem Rezeptor auf den Nervenfasern zu stören, um diese aus ihrer Gefangenschaft an der Verletzungsstelle zu befreien“, so Fischer. Ob ähnliche Ansätze auch in anderen Bereichen des verletzten Gehirns oder Rückenmarks die Regeneration von Axonen fördern können, ist Gegenstand aktueller Untersuchungen seines Teams am Lehrstuhl für Zellphysiologie.
Das Team der Zellphysiologie um Prof. Dr. Dietmar Fischer berichtet in der Zeitschrift Proceedings of the National Academy of Science PNAS vom 25. Mai 2021, online vorab.
Originalpublikation:
Alexander M. Hilla, Annemarie Baehr, Marco Leibinger, Anastasia Andreadaki, Dietmar Fischer: CXCR4/CXCL12-mediated entrapment of axons at the injury site compromises optic nerve regeneration, in: PNAS, 2021, DOI: 10.1073/pnas.2016409118
Quelle: RUB