Limbusstammzellinsuffizienz: Können wir die Hornhaut bald mit Stammzellen reparieren?
Wegen des weltweiten Mangels an Spendergewebe ruhen auf der Entwicklung einer künstlichen Hornhaut mithilfe von Stammzellen große Hoffnungen. Professor Dr. rer. nat. Ursula Schlötzer-Schrehardt, Leiterin der Forschungsabteilung an der Augenklinik der Universität Erlangen-Nürnberg, über den aktuellen Stand der Forschung, den sie auf der DOG 2021 vorgestellt hat.
1. Hintergrund
Angesichts eines weltweiten Mangels an Spendergewebe werden große Forschungsbemühungen in die Entwicklung einer künstlichen Hornhaut mithilfe von Stammzellen gesteckt. In der klinischen Anwendung befinden sich momentan aber nur Behandlungsansätze zum Ersatz der äußersten Zellschicht der Hornhaut, des Hornhautepithels, dessen Schädigung zum Verlust der Sehfunktion führen und das mit Hilfe von Stammzellen regeneriert werden kann.
2. Was sind Stammzellen?
Stammzellen sind bei jedem Menschen ein Leben lang kontinuierlich im Einsatz. Sie teilen und vermehren sich unbegrenzt und sind maßgeblich an den ständigen Erneuerungsprozessen im Körper beteiligt, indem sie verbrauchtes oder verletztes Gewebe regenerieren. Diese einzigartige Fähigkeit wird von modernen Stammzelltherapien genutzt, um einzelne Gewebe oder eines Tages vielleicht auch ganze Organe regenerieren zu können.
3. Stammzellen in der Hornhaut
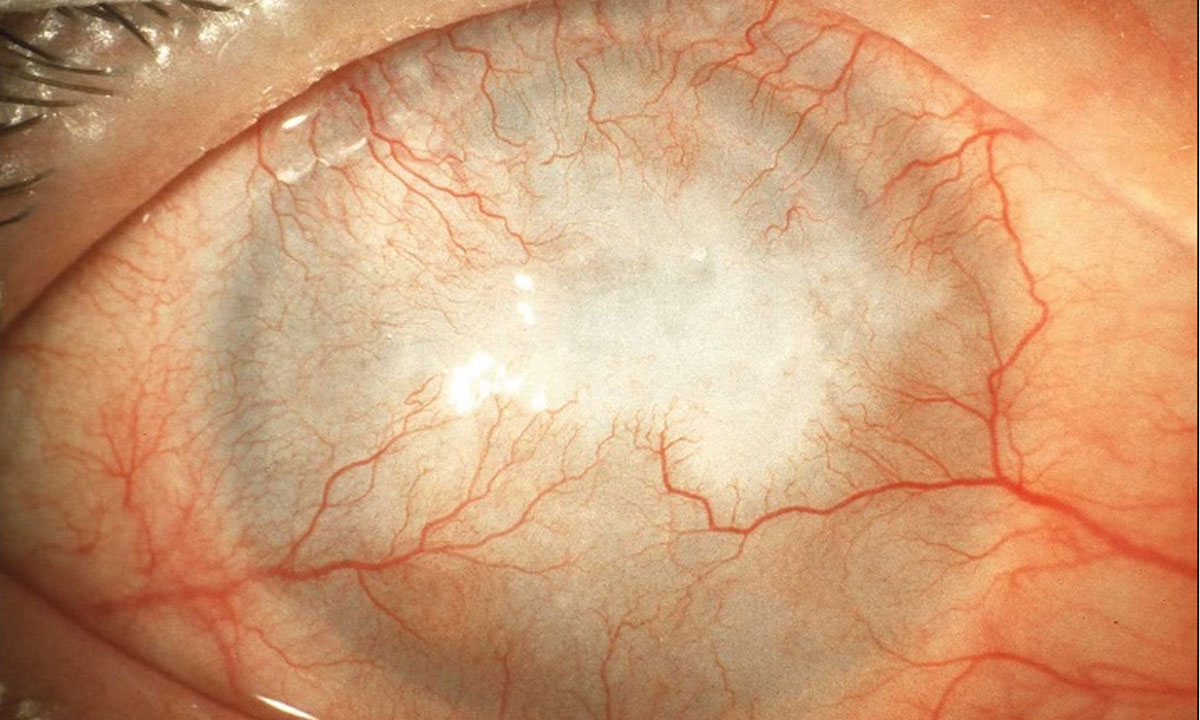
Stammzellen sind auch in der Limbusregion des Auges, am Rand der Hornhaut, vorhanden, wo sie ein Leben lang für die kontinuierliche Erneuerung des Hornhautepithels und somit für die Aufrechterhaltung der Sehfunktion verantwortlich sind. Sind diese sogenannten limbalen Stammzellen durch Verletzungen oder Erkrankungen nicht mehr funktionstüchtig, kann eine reguläre Hornhautregeneration nicht mehr stattfinden und es kommt zur Eintrübung der Hornhaut durch Überwachsen der Bindehaut („Konjunktivalisierung“).
Das daraus resultierende Krankheitsbild der Limbusstammzellinsuffizienz ist eine zwar relativ seltene, aber schwere Erkrankung der Augenoberfläche mit einer geschätzten Häufigkeit von 20/100.000 (www.orphanet.net). Sie kann nicht nur nach Verletzungen oder im Rahmen verschiedener Erkrankungen, sondern auch bei chronischem Trockenem Auge oder nach langjährigem Tragen von Kontaktlinsen auftreten. Die Betroffenen klagen über schmerzhaften Sehverlust bis hin zur vollständigen Erblindung.
4. Therapie der Limbusstammzellinsuffizienz
Zur Therapie einer fortgeschrittenen Limbusstammzellinsuffizienz und Rekonstruktion der Hornhautoberfläche ist eine Übertragung gesunder Stammzellen in einem Transplantat notwendig. Hierfür stehen verschiedene Verfahren der Stammzelltransplantation zur Verfügung, wobei sich die Kultivierung von limbalen Stammzellen, die aus einem kleinen Gewebebiopsat gewonnen werden, seit Ende der 1990er-Jahre zu einer gewebeschonenden, weit verbreiteten Behandlungsoption entwickelt hat.
Hierfür werden limbale Stammzellen vom gesunden Partnerauge des Patienten (autologe Transplantation) oder von einer Spenderhornhaut (allogene Transplantation) entnommen, im Zellkulturlabor auf unterschiedlichen Trägern (zum Beispiel Fibringel, Amnionmembran) vermehrt und anschließend auf das erkrankte Auge transplantiert. Mittlerweile liegen Erfahrungen aus über 20 Jahren klinischer Anwendung mit Erfolgsraten von etwa 70 Prozent nach autologer Stammzelltransplantation vor, während die Ergebnisse nach allogener Limbusstammzelltransplantation allerdings wesentlich ungünstiger ausfallen.
Dem daraus entwickelten Gewebeprodukt Holoclar® (Chiesi Farmaceutici), bestehend aus einem Fibringel als Träger und autologen kultivierten Limbusstammzellen, wurde bereits 2015 eine bedingte EU-Zulassung als Arzneimittel für die Behandlung einer einseitigen Limbusstammzellinsuffizienz nach Verätzung oder Verbrennung erteilt. Damit repräsentiert Holoclar® die erste kommerzielle Stammzelltherapie für das Auge in der Europäischen Union. Die Zahl der behandelbaren Patienten ist allerdings gering - in ganz Europa kommen jährlich kaum mehr als tausend Fälle in Frage. Die finale Auswertung der multizentrischen, multinationalen, prospektiven klinischen Studie wird Ende 2021 erwartet. Mittlerweile wurde 2020 in Japan ein ähnliches zellbasiertes Medizinprodukt, „Nepic“ („Autologous Cultured Corneal Epidermis“; J-TEC), zur Behandlung einer einseitigen Limbusstammzellerkrankung zugelassen.
Nicht immer steht jedoch ein gesundes Partnerauge zur Entnahme einer Limbusbiopsie zur Verfügung. Sind beide Augen in Mitleidenschaft gezogen, muss man auf Limbusstammzellen aus Spenderhornhäuten oder, um Abstoßungsreaktionen zu vermeiden, auf Stammzellen aus anderen patienteneigenen Geweben zurückgreifen. In der klinischen Anwendung sind patienteneigene Stammzellen aus dem Epithel der Mundschleimhaut, die in der Kulturschale in ein Hornhautepithel-Äquivalent zur Rekonstruktion der Augenoberfläche gezüchtet werden. Erst kürzlich wurde das daraus resultierende Medizinprodukt „Ocural“ („Autologous Cultured Oral Mucosal Epithelium“; J-TEC) für die Behandlung einer beidseitigen Limbusstammzellerkrankung in Japan zugelassen.
Ganz aktuell wurde ein weiteres Stammzell-basiertes Zelltherapeutikum, bestehend aus ABCB5-positiven allogenen Limbusstammzellen, die aus einer Spenderhornhaut isoliert und unter GMP-Bedingungen kontrolliert angereichert werden, vorgestellt. „ABCB5“ steht dabei für ein Membranprotein, das ATP binden und Moleküle aktiv durch die Zellmembran der Stammzellen transportieren kann. Nach der Zulassung des neuen Arzneimittelprodukts durch die US-amerikanische Gesundheitsbehörde (FDA) und die Europäische Arzneimittelbehörde (EMA) wird es zurzeit in einer internationalen, multizentrischen klinischen Studie geprüft und könnte bald als neue Therapieoption für Patienten mit beidseitiger Limbusstammzellinsuffizienz zur Verfügung stehen.
Insgesamt gilt die Transplantation von aus Stammzellen gezüchtetem Limbus- oder Mundschleimhautepithel als ein etabliertes und sicheres klinisches Verfahren mit hohen Erfolgsraten für eine transiente Stabilisierung der Augenoberfläche und Visusverbesserung für die Patienten. Die Langzeitergebnisse der aktuellen Therapieansätze sind jedoch noch nicht gänzlich zufriedenstellend, was die Notwendigkeit zur Neu- und Weiterentwicklung regenerativer Stammzelltherapien unterstreicht.
5. Neue Therapieansätze
Mögliche Ursachen für die Limitationen der aktuellen Behandlungsansätze im Langzeitverlauf könnten in der zu geringen Anzahl der transplantierten Stamm- und Vorläuferzellen liegen, da angenommen wird, dass der langfristige klinische Erfolg vom Erhalt der Stammzellen im Transplantat bestimmt wird. Stammzellen befinden sich in vivo an geschützten Orten, den Stammzellnischen, wo sie vor Differenzierung und Alterung geschützt und in einem teilungsfähigen Zustand erhalten werden. Sobald sie aber aus ihrer physiologischen Nische entfernt werden, wie es im Rahmen der gängigen Kultivierungsverfahren und Therapieansätze geschieht, können sie im Transplantat nicht langfristig überleben und gehen verloren. Ihre Differenzierung zu Gewebezellen setzt unwiderruflich ein, so dass das Regenerationspotenzial bald erschöpft ist.
Ein primäres Ziel moderner regenerativer Stammzelltherapien ist es demnach, die physiologische Stammzellnische in der Kulturschale nachzuahmen, um die Stammzellfunktionen im Transplantat aufrechtzuerhalten. Daher zielen unsere aktuellen Forschungsaktivitäten darauf ab, die Zusammensetzung der Limbusstammzellnische zu analysieren, um Schlüsselfaktoren der Nische, wie beispielsweise Extrazellulärmatrix oder unterstützende Nischenzellen, im Transplantat nachzubilden. Ein Beispiel hierfür: Wir entwickeln aktuell biotechnologisch standardisierte Zellträger, sogenannte Hydrogele, basierend auf Fibrin und Hyaluronsäure, die eine wichtige Komponente der physiologischen Nische bildet. In diese Hydrogele inkorporieren wir neben den eigentlichen Stammzellen auch verschiedene Nischenzellen, die die Stammzellen unterstützen und am Leben erhalten. Die auf diese Weise gezüchteten „biomimetischen“ Epithelkonstrukte können nicht nur die Stammzellen bewahren, sondern zeigen auch eine verbesserte strukturelle Organisation als herkömmliche Transplantate.
Für Patienten mit beidseitiger Erkrankung ohne eigene intakte Limbusstammzellen untersuchen Forscher derzeit die Eignung von Stammzellen aus Haarfollikeln oder aus der Zahnpulpa, von embryonalen Stammzellen sowie von induzierten pluripotenten Stammzellen (iPS), um daraus im Labor Hornhautepithelkonstrukte zu generieren. Auch hierbei können Schlüsselfaktoren der Limbusnische die Transdifferenzierung in Limbusstammzellen unterstützen.
In Japan haben Mediziner erstmals Hornhautepithelgewebe transplantiert, das aus allogenen iPS-Zellen gezüchtet wurde. iPS-Zellen sind ausgereifte Körperzellen, zum Beispiel aus der Haut, die in der Kulturschale zu Stammzellen zurückprogrammiert und in Hornhautepithelzellen umprogrammiert wurden. In einer laufenden klinischen Studie werden Wirksamkeit und Sicherheit dieses neuen Behandlungskonzepts untersucht. Im Falle eines Erfolges hätte man mit den iPS-Zellen eine theoretisch unerschöpfliche Quelle von Stammzellen für den Hornhautepithelersatz zur Verfügung.
6. Ausblick
Seit Jahren schon gelten Stammzellen als die Hoffnungsträger in der regenerativen Medizin. Auch den limbalen Stammzellen der Hornhaut wurde ein großes Potenzial für die Rekonstruktion der Augenoberfläche zugeschrieben, was zur Entwicklung der ersten in Europa zugelassenen und kommerziell verfügbaren Stammzelltherapie (Holoclar®) geführt hat. Allerdings steht sie nur einer kleinen Anzahl von ausgewählten Patienten zur Verfügung; auch steht der endgültige Studienbericht noch aus. Leider sind aktuell auch keine guten Therapieoptionen für die weitaus größere Gruppe von Patienten mit beidseitiger Limbusstammzellerkrankung verfügbar, denn nach Transplantation von kultiviertem Mundschleimhautepithel bleibt das Wiederauftreten von Hornhautvaskularisationen ein Problem. Auch chronische Begleiterkrankungen, wie Tränenfilmstörungen und Entzündungen, machen einen Transplantationserfolg häufig zunichte. Das Warten auf den großen Durchbruch zur Wiederherstellung einer gesunden Augenoberfläche ist demnach noch lange nicht zu Ende und an realistische Alternativen für Hornhautspenden für Gewebetransplantationen ist noch lange nicht zu denken.
Daher besteht nach wie vor großer Bedarf an einer Weiterentwicklung der bestehenden Therapieverfahren, wobei das Konzept der Stammzellnische immer mehr an Bedeutung gewinnt, nicht nur für den Erhalt der Stammzellen im Transplantat, sondern auch für die Regeneration des geschädigten Mikromilieus nach der Transplantation. Entscheidend für zukünftige Entwicklungen wird sein, die Regulation der Stammzellen und ihrer Nische besser zu verstehen, um die regenerativen Zelltherapien und die klinischen Langzeitergebnisse nachhaltig zu verbessern.
Professor Dr. rer. nat. Ursula Schlötzer-Schrehardt
Leiterin der Forschungsabteilung
Augenklinik der Universität Erlangen-Nürnberg